Pozadina i dizajn studije
Retatrutid (LY3437943) je novi lijek s jednim peptidom koji aktiviratri receptora istovremeno: GIP, GLP-1 i glukagon. Da bi se procijenila njegova efikasnost i sigurnost kod osoba s gojaznošću, ali bez dijabetesa, provedeno je randomizirano, dvostruko slijepo, placebom kontrolirano ispitivanje faze 2 (NCT04881760). Ukupno338 učesnikasa BMI ≥30 ili ≥27 sa najmanje jednom komorbiditetom povezanom s težinom, bili su nasumično raspoređeni da primaju placebo ili retatrutid (1 mg, 4 mg sa dva titracijska rasporeda, 8 mg sa dva titracijska rasporeda ili 12 mg) koji se primjenjivao jednom sedmično potkožnom injekcijom tokom 48 sedmica.primarni ciljbila je procentualna promjena tjelesne težine nakon 24 sedmice, sa sekundarnim krajnjim tačkama koje su uključivale promjenu težine nakon 48 sedmica i kategoričke pragove gubitka težine (≥5%, ≥10%, ≥15%).
Ključni rezultati
-
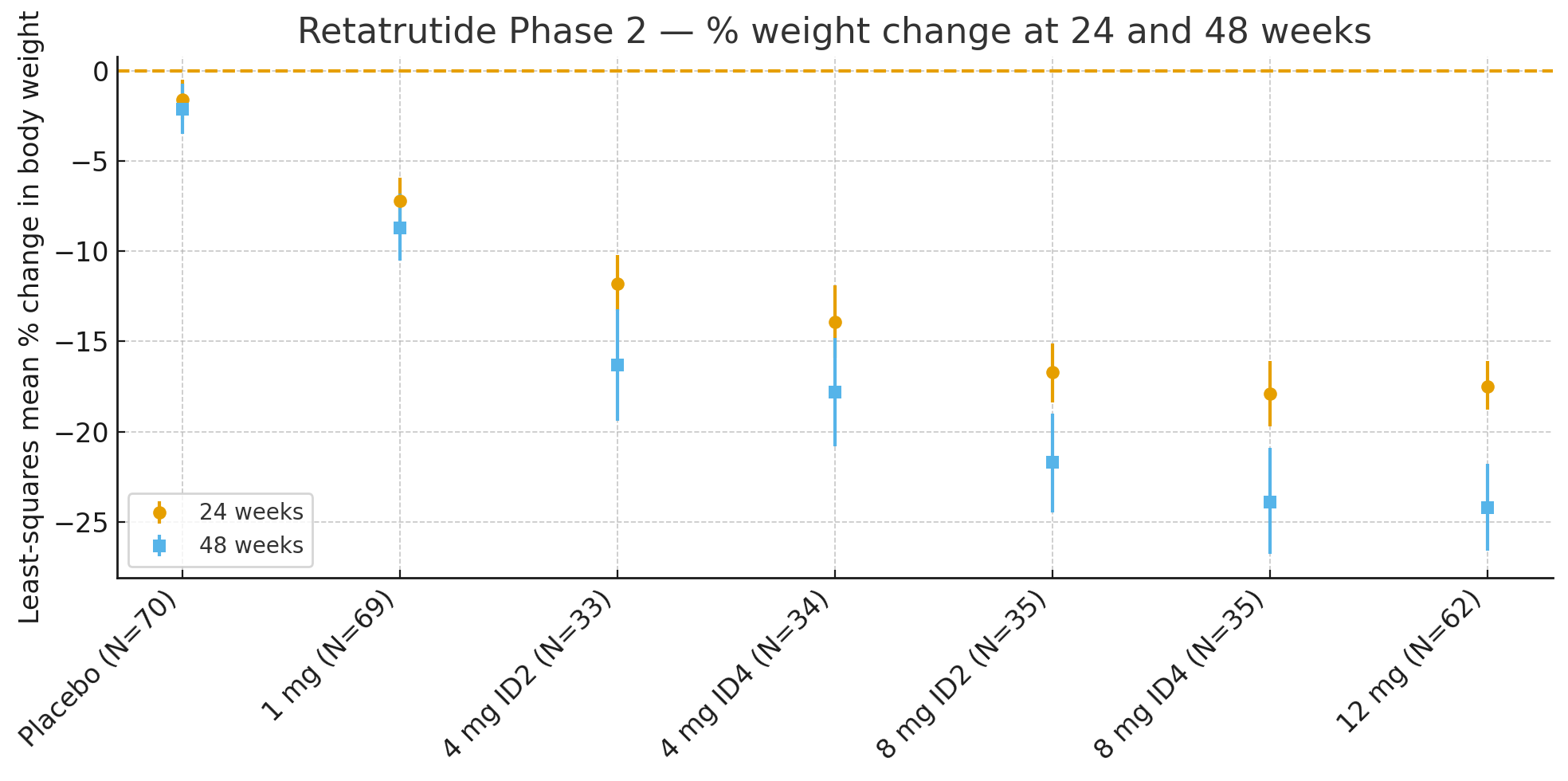
24 sedmice: Srednja procentualna promjena tjelesne težine u odnosu na početnu vrijednost izračunata metodom najmanjih kvadrata bila je
-
Placebo: −1,6%
-
1 mg: −7,2%
-
4 mg (kombinovano): −12,9%
-
8 mg (kombinovano): −17,3%
-
12 mg: −17,5%
-
-
48 sedmicaProcenat promjene tjelesne težine bio je
-
Placebo: −2,1%
-
1 mg: −8,7%
-
4 mg (kombinovano): −17,1%
-
8 mg (kombinovano): −22,8%
-
12 mg: −24,2%
-
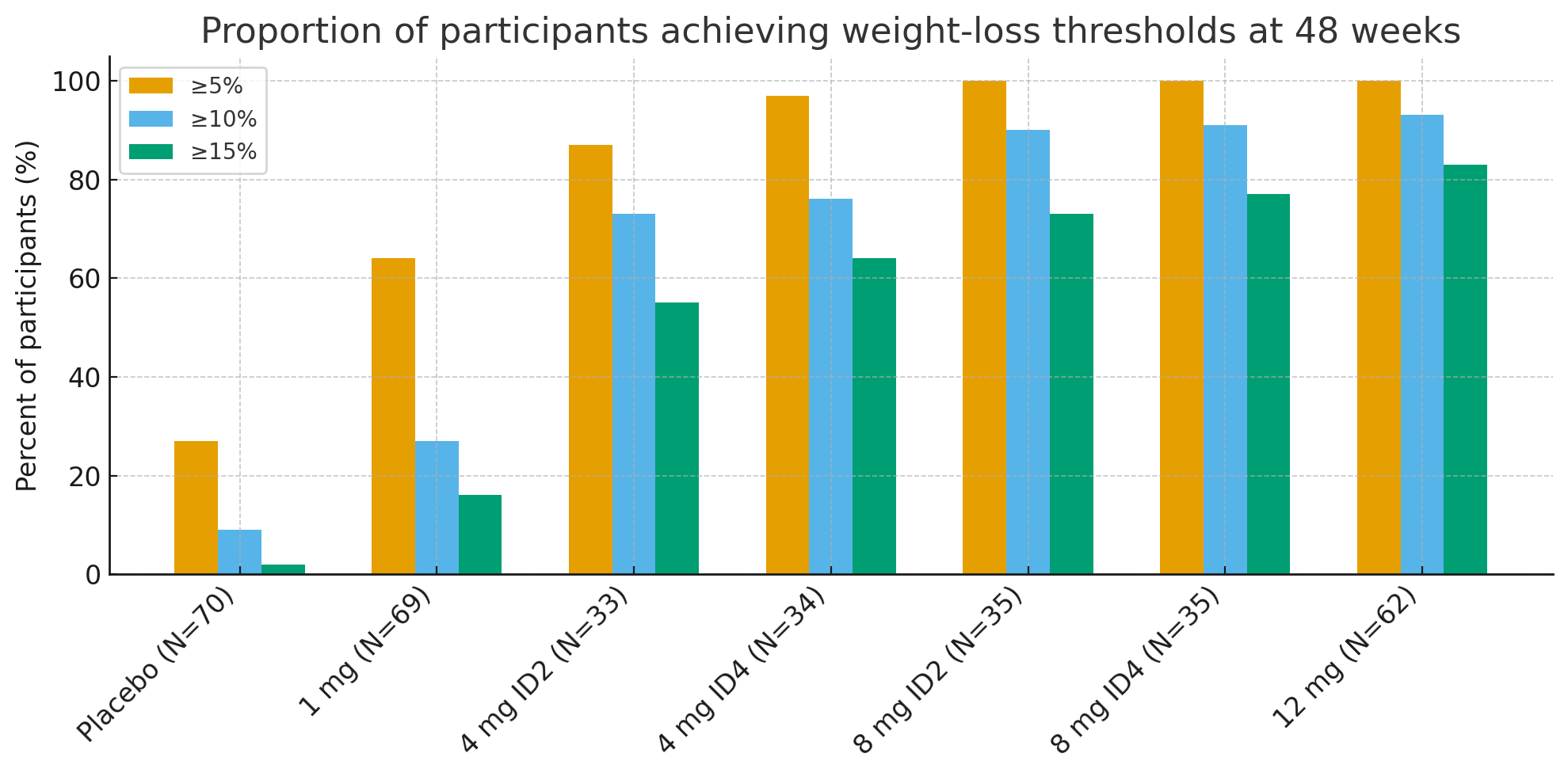
Nakon 48 sedmica, udio učesnika koji su postigli klinički značajne pragove gubitka težine bio je zapanjujući:
-
Gubitak težine ≥5%: 27% s placebom u odnosu na 92–100% u aktivnim grupama
-
≥10%: 9% s placebom u odnosu na 73–93% u aktivnim grupama
-
≥15%: 2% s placebom u odnosu na 55–83% u aktivnim grupama
U grupi od 12 mg, do26% učesnika je izgubilo ≥30% svoje početne težine, obim gubitka težine uporediv sa barijatrijskom hirurgijom.
Sigurnost
Najčešći neželjeni događaji bili su gastrointestinalni (mučnina, povraćanje, dijareja), uglavnom blagi do umjereni i zavisni od doze. Niže početne doze (titracija od 2 mg) smanjile su ove događaje. Uočeno je povećanje srčanog ritma povezano s dozom, koje je dostiglo vrhunac u 24. sedmici, a zatim je opadalo. Stope prekida liječenja kretale su se od 6-16% u aktivnim grupama, što je nešto više nego kod placeba.
Zaključci
Kod odraslih osoba s gojaznošću bez dijabetesa, sedmična subkutana primjena retatrutida tokom 48 sedmica proizvela jeznačajno, od doze ovisno smanjenje tjelesne težine(do ~24% prosječnog gubitka pri najvišoj dozi), uz poboljšanja kardiometaboličkih markera. Gastrointestinalni neželjeni događaji bili su česti, ali su se mogli upravljati titracijom. Ovi nalazi faze 2 ukazuju na to da bi retatrutid mogao predstavljati novi terapijski kriterij za gojaznost, uz potvrdu u većim, dugoročnim ispitivanjima faze 3.
Vrijeme objave: 28. septembar 2025.